(12分)在一定条件下,存在如下反应:2SO2(g)+ O2 (g)  2SO3(g);ΔH<0
2SO3(g);ΔH<0
(1)写出该反应的化学平衡常数表达式K=
(2)升高温度,该反应K值 ,SO2转化率 ,正反
应速率 (填增大、减小或不变)
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是
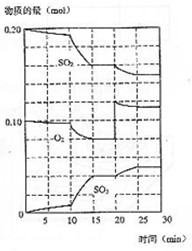
(4)据图判断,反应进行至20min时,曲线发生变化的原因
是___________________(用文字表达),10min到15min的曲线变化的原因可能是 (填编号)。
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加SO3物质的量(5)在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_______性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__ ____ 。
(12分)
(1)(1分)
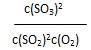
6.减小、减小、增大 (各1分,共3分)(3)15-20min和25-30min (2分)
(4)增大O2浓度(通入O2)(1分) AB(2分)
(5)中(1分) Kb=10-9/(a-0.01)mol·L-1.(单位不算分,2分)