问题
填空题
(13分)工业合成氨是硝酸工业中的重要步骤,已知N2(g) +3H2(g)  2NH3(g) ΔH=-92.4kJ·mol-1。请回答:
2NH3(g) ΔH=-92.4kJ·mol-1。请回答:
(1) 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、 H2和NH3的量),反应速率与时间的关系如右图所示。
H2和NH3的量),反应速率与时间的关系如右图所示。

图中t1时引起平衡移动的条件可能是 __ , t3时引起平衡移动的条件可能是 __ ___ , 其中表示平衡混合物中NH3的含量最高的一段时间是 。
(2) 温度为T ℃时,将2a mol H2和a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该反应的化学平衡常数的值为 ___________________。请在答题卷上写出具体的计算过程。
答案
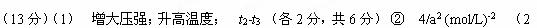
N2(g) + 3H2(g)  2NH3(g)
2NH3(g)
起始物质的量浓度(mol.L-1) 2a 4a 0
物质的浓度变化(mol.L-1) a 3a 2a
平衡物质的量浓度(mol.L-1) a a 2a (3分)
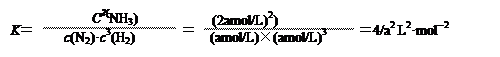 (2分)
(2分)

