在一个体积为2L的密闭容器中,高温下发生下列反应:
Fe(s) + CO2(g) FeO(s) + CO(g) + Q kJ
FeO(s) + CO(g) + Q kJ
其中CO2、CO的物质的量(mol)随时间(min)的变化如图所示。
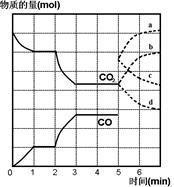
(1)、反应在1min时第一次达到平衡状态,固体的质量增加了3.2g。用CO的浓度变化表示的反应速率υ(CO)=_________。
(2)、反应进行至2min时,若只改变一个条件,曲线发生的变化如图所示,3min时再次达到平衡,则Q 0(填“>”、“<”或“=”)。第一次平衡与第二次平衡的平衡常数相比,K1 K2。(填“>”、“<”或“=”)。
(3)、5min时再充入一定量的CO(g),平衡发生移动。下列说法正确的是 (填写编号)。
a.υ(正)先增大后减小 b.υ(正)先减小后增大
c.υ(逆)先增大后减小 d.υ(逆)先减小后增大
表示n(CO2)变化的曲线是________(填写图中曲线的字母编号)。
(4)、请用固态物质的有关物理量来说明该反应已经达到化学平衡状态:
______________________________________________________________________。
0.1mol/(L·min)(2分)
<;<(1分1答,共2分)
c ; b (1分1答,共2分)
Fe(或FeO)的质量(或物质的量)保持不变;固体总质量保持不变。(2分)
(1)、固体的质量增加了3.2g,根据化学反应方程式,可知有0.2mol FeO生成,即在1min内也生成了0.2molCO,υ(CO)= 0.1mol/(L·min)
(2)反应进行至2min时,改变的条件是升温,因为反应速率加快,平衡右移,正反应是吸热反应,Q<0,升温,平衡右移,K增大,所以K1 <K2
(3) 5min时再充入一定量的CO(g),平衡向左移动,υ(逆)突然增大,然后减小,υ(正)逐渐增大,故选C。
表示n(CO2)变化的曲线是b,平衡左移,n(CO2)逐渐增大。
(4) Fe(或FeO)的质量(或物质的量)保持不变;固体总质量保持不变,就能说明可逆反应已经达到化学平衡状态。
