问题
填空题
.(9分)在0.l mol·L-1的CH3COOH溶液中存在如下电离平衡:CH3COOH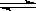 CH3COO-+H+,请根据该平衡完成下列表格,电离平衡移动方向填“正方向”或“逆方向”,离子浓度的变化请用“增大”、“减小”或“不变”表示。
CH3COO-+H+,请根据该平衡完成下列表格,电离平衡移动方向填“正方向”或“逆方向”,离子浓度的变化请用“增大”、“减小”或“不变”表示。
| 改变条件 | 电离平衡移动方向 | c(H+) | c(CH3COO-) |
| 加水稀释 | |||
| 加少量冰醋酸 | |||
| 加入少量CH3COONa固体 |
答案
(9分)每空1分
| 改变条件 | 电离平衡移动方向 | c(H+) | c(CH3COO-) |
| 加水稀释 | 正方向 | 减小 | 减小 |
| 加少量冰醋酸 | 正方向 | 增大 | 增大 |
| 加入少量CH3COONa固体 | 逆方向 | 减小 | 增大 |
弱电解质的电离平衡受温度、浓度、酸、碱及盐等的影响;
(1)加水稀释,平衡正向移动,促进电离,但c(H+)、c(CH3COO-)均减小,电解程度增大
(2)加入少量冰醋酸,增大反应物浓度,平衡正向移动,c(H+)、c(CH3COO-)均增大,但电解质电离程度减小
(3)加入少量CH3COONa固体,c(CH3COO-)增大,平衡左移,c(H+)减小
