(11分)用中和滴定法确定某烧碱样品的浓度,试根据实验回答下列问题:
(1)滴定时,用0.2000mol·L-1的盐酸来滴定待测溶液,不可选用 (填编号字母)作指示剂。
(A)甲基橙 (B)石蕊 (C)酚酞
(2)若选用甲基橙作指示剂,滴定终点的判断方法是
,此时溶液显 性。
(3)根据下表数据,计算被测烧碱溶液的物质的量浓度是 mol·L-1。]
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
| 第三次 | 10.00 | 0.40 | 21.50 |
(4)分析下列实验操作会对滴定结果产生的影响。(填“偏高”、“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果 。
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果 。
③若烧碱溶液隔夜后滴定,选用甲基橙作指示剂时,则滴定结果 。
(1) (B) (2) 当加入最后一滴标准的酸液时,溶液刚好由黄色变为橙色,且半分钟内不褪色 酸 (3) 0.4000 (4)① 偏高 ② 偏高 ③无影响 (各2分)
(1)因为石蕊试液的颜色变化不明显,不便于观察,所以不能选用石蕊试液作指示剂。
(2)甲基橙的变色范围是3.1~4.4,即溶液是显酸性的。所以盐酸滴定碱液终点的变化是当加入最后一滴标准的酸液时,溶液刚好由黄色变为橙色,且半分钟内不褪色。
(3)三次实验中消耗盐酸的体积分别为20.10ml、19.90ml、21.10ml,所以第三次的实验误差大,所以取前2次的平均值,即盐酸的体积是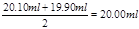 ,所以烧碱溶液的物质的量浓度是
,所以烧碱溶液的物质的量浓度是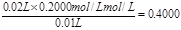 。
。
(4)开始俯视,则读数偏小,滴定终点平视,所以最终盐酸的体积偏大,结果偏高。锥形瓶用待测液润洗,则氢氧化钠的量偏多,消耗盐酸的体积偏大,结果偏高。烧碱溶液隔夜后滴定,则会含有杂质碳酸钠,但甲基橙的变色范围是在酸性环境中,所以根据原子守恒可知,消耗的盐酸是相同,不影响测定结果。
