(10分)将1mol CO和1mol H2O充入某固定容积的反应器中,在某条件下达到平衡:CO+H2O(g)?CO2+H2,此时有2/3的CO转化为CO2。
(1)该平衡混合物中CO2的体积分数为__________。
(2)若在相同条件下,向容器中充入1mol CO2、1mol H2和1mol H2O,则达到平衡时与(1)中平衡相比较,平衡应向__________(填“正反应方向”、“逆反应方向”或“不”)移动,此时平衡混合物中CO2的体积分数可能是下列各值中的__________
A.22.2%
B.27.55%
C.33.3%
D.36.8%(3)结合(2)中计算结果分析若平衡向正反应方向移动时,则下列说法中正确的是__________。
①生成物的产量一定增加;②生成物的体积分数一定增加;③反应物的转化率一定增大;④反应物的浓度一定降低;⑤正反应速率一定大于逆反应速率;⑥一定使用了催化剂
(10分)(1)33.3% (3分)(2)正反应方向(2分);B (3分)(3)①⑤(2分)
(1)设CO的浓度变化为x,由化学反应方程式;
CO +H2O(g)?CO2+H2
起始物质的量 1 1 0 0
变化物质的量 2/3 2/3 2/3 2/3
平衡物质的量 1/3 1/3 2/3 2/3
平衡混合物中CO2的体积分数为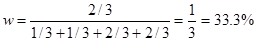
(2)在相同条件下,向容器中充入1mol CO2、1mol H2和1mol H2O相当于在(1)达到平衡的基础上再加入1mol H2O,即平衡将向着正反应的方向移动;
若CO完全转化成CO2,即反应后CO2的物质的量为1mol,由于该反应为等体积反应,所以平衡后混合物中CO2的体积分数为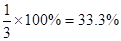 ,而实际上CO不可能完全转化为CO2,所以答案只能从A、B中选择。
,而实际上CO不可能完全转化为CO2,所以答案只能从A、B中选择。
若有2/3的CO转化为CO2,即反应后CO2的物质的量为2/3mol,平衡后混合物中CO2的体积分数为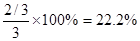 ,而实际上CO的转化率要大于(1)中CO的转化率,所以正确的答案为B。
,而实际上CO的转化率要大于(1)中CO的转化率,所以正确的答案为B。
(3)由于平衡向正反应方向移动,生成物的产量一定增加①正确;生成物的体积分数减小②错;反应物的转化率H2O减小③错;反应物的浓度不一定降低,如H2O(g)④错;⑤正确,因为反应向正反应方向移动;⑥错,加入了催化剂只能加快反应速率,对平衡的移动无影响。
