问题
选择题
已知:N2(g)+3H2(g) 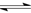 2NH3(g) △H =-92.4 kJ·mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) △H =-92.4 kJ·mol-1,在温度、容积相同的2个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 容器1 | 容器2 |
| 反应物投入量始态 | 1mol N2、3mol H2 | 2mol NH3 |
| NH3的平衡浓度/mol·L-1 | cl | c2 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ |
| 体系压强/Pa | p1 | p2 |
| 反应物转化率 | α1 | α2 |
A. cl 一定等于c2 B.a + b = 92.4
C. p1 一定等于p2 D.α1 一定等于α2
答案
答案:D
因为恒温恒容,体积可变的反应,容器1和2中是从不同方向进行的等效平衡,ABC正确,因为进行的方向不同α1 不等于α2
