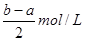问题
计算题
向2L密闭容器中通入amol 气体A和bmol气体B,在一定条件下发生反应:
xA(g)+yB(g) 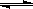 pC(g)+qD(g)
pC(g)+qD(g)
已知:平均反应速率vC=vA/2;反应2min 时,A的物质的量减少了1/3,B的物质的量减
少了a/2 mol,有a mol D生成。请计算回答:(写出计算过程)
(1)反应2min内,v(A) =__________________
(2)化学方程式中,x= 、y= 、p= 、q= 。
(3)平衡时,D为 2a mol,此时B的物质的量浓度为?
答案
(1) (2) 2 3 1 6 (3)
(2) 2 3 1 6 (3)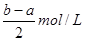
平均反应速率vC=vA/2,所以x︰p=2︰1。反应2min 时,A的物质的量减少了1/3,B的物质的量减少了a/2 mol,有a mol D,所以x︰y︰q=2︰3︰6,即x︰y︰p︰q=2︰3︰1︰6。反应2min内,v(A)=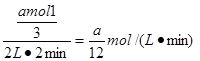 。
。
2A(g)+3B(g) 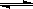 C(g)+6D(g)
C(g)+6D(g)
起始量(mol) a b 0 0
转化量(mol) 2ª/3 a a/3 2ª
平衡量(mol) a/3 (b-a) a/3 2ª
所以平衡时B的物质的量浓度为