问题
选择题
强酸与强碱的稀溶液发生中和反应的热化学方程式:H+(aq)+OH-(aq)=H2O(1) ⊿H=-57.3kJ/mol。向1L1mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的反应热⊿H1、⊿H2、⊿H3的关系正确的是( )
A.⊿H1>⊿H2>⊿H3
B.⊿H1<⊿H3<⊿H2
C.⊿H1<⊿H2<⊿H3
D.⊿H1>⊿H3>⊿H2
答案
答案:D
醋酸是弱电解质,存在电离平衡,电离是吸热的,因此放出的热量少。浓硫酸溶于水放出大量的热,由于放热越多,△H越小,因此正确的答案选D。

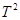 为纵坐标,将所得数据连成直线如图B所示,利用图像可求出重力加速度g=_______
为纵坐标,将所得数据连成直线如图B所示,利用图像可求出重力加速度g=_______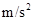 。(结果保留三位有效数字)
。(结果保留三位有效数字)