问题
计算题
(共10分)已知合成氨反应为:N2 + 3H2 2NH3,在一定温度下,向2L密闭容器中,加入2molN2和5molH2,一定条件下使之反应,经过2min后达到平衡状态并测得NH3为0.4mol,求:
2NH3,在一定温度下,向2L密闭容器中,加入2molN2和5molH2,一定条件下使之反应,经过2min后达到平衡状态并测得NH3为0.4mol,求:
(1)以N2表示这2min内该反应的反应速率?
(2)此时氢气的转化率?
(3)平衡时NH3的体积分数?(保留1位小数)
(4)平衡时容器中的压强与开始压强之比?
(5)平衡时容器中气体的平均摩尔质量?
答案
(1)0.05 mol/L.min (2)12% (3)6.7% (4)33/35 (5)10g/mol
N2 + 3H2 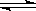 2NH3
2NH3
2mol 5mol 0
0.2mol 0.6mol 0.4mol
1.8mol 4.4mol 0.4mol
V(N2)=0.2mol/2L.2min=0.05 mol/L.min ﹠H2=0.6mol/5mol=12%
NH3℅=0.4mol/6.6mol="6.7%" p2/p1=n2/n1=6.6mol/7mol="33/35"
M=m/n=(28×2+5×2)/6.6mol=10g/mol
