问题
选择题
在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1, c(C)="0" mol·L-1。反应物A的浓度随时间的变化如图所示。下列说法正确的是
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1, c(C)="0" mol·L-1。反应物A的浓度随时间的变化如图所示。下列说法正确的是
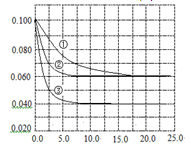
A.若反应①、②的平衡常数分别为K1、K2,则K1< K2
B.反应A+2B C的△H>0
C的△H>0
C.实验②平衡时B的转化率为60%
D.减小反应③的压强,可以使平衡时c(A)="0.060" mol·L-1
答案
答案:B
反应①②中平衡时A的浓度是相同的,说明①和②的平衡状态是相同的,因此平衡常数相同。根据图像可知反应③的反应速率最快,说明溶液的温度高。但平衡时A的浓度最小,这说明升高温度平衡向正反应方向移动,所以正反应是吸热反应,B正确。在实验②中平衡时A的浓度是0.060mol/L,所以A的浓度变化量是0.040mol/L,因此B的浓度变化量是0.080mol/L,所以B的转化率是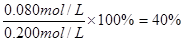 。反应物和生成物不是气体,所以改变压强不会影响平衡状态。答案选B。
。反应物和生成物不是气体,所以改变压强不会影响平衡状态。答案选B。
