问题
选择题
将一定质量的Ag2SO4固体置于容积不变的密闭容器中(加入少量V2O5),在某温度时发生下列反应:Ag2SO4(s) Ag2O(s)+SO3(g),2SO3(g)
Ag2O(s)+SO3(g),2SO3(g) 2SO2(g)+O2(g)。10min后反应达到平衡,此时c(SO3)为0.4mol·L-1、c(SO2)为0.1mol·L-1,则下列叙述中不正确的是( )
2SO2(g)+O2(g)。10min后反应达到平衡,此时c(SO3)为0.4mol·L-1、c(SO2)为0.1mol·L-1,则下列叙述中不正确的是( )
A.SO3的分解率为20%
B.容器内气体的密度为40g/L
C.达到平衡时分解的Ag2SO4固体为0.5mol
D.10min内用O2表示的该反应的反应速率为0.005mol/(L·min)
答案
答案:C
c(SO2)为0.1mol·L-1,则消耗的三氧化硫是0.1mol·L-1,所以三氧化硫的起始浓度是0.1mol·L-1+0.4mol·L-1=0.5mol·L-1,因此分解率是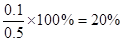 ,A正确。密度是气体的质量和容器容积的比值,所以密度是
,A正确。密度是气体的质量和容器容积的比值,所以密度是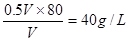 ,B正确。C不正确,因为容器的容积无法确定。平衡时氧气的浓度是0.05mol·L-1,所以用氧气表示的反应速率是
,B正确。C不正确,因为容器的容积无法确定。平衡时氧气的浓度是0.05mol·L-1,所以用氧气表示的反应速率是
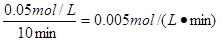 ,D正确,答案选C。
,D正确,答案选C。
