(6分)在某温度下,将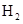 和
和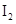 各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定
各0.1mol的气态混合物充入10L的密闭容器中,充分反应,连续测定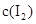 的变化,5S时测定
的变化,5S时测定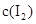 =0.0080mol/L并保持不变。H2+I2(g)
=0.0080mol/L并保持不变。H2+I2(g)  2HI(g)
2HI(g)
(1)反应的平衡常数的表达式是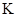 = ;
= ;
(2)此温度下,平衡常数值为 ;
(3)若在此温度下,在10L的密闭器充入0.2molHI气体,达到平衡时,HI的转化率为 。
(1) (2) 0.25 (3) 80%
(2) 0.25 (3) 80%
(1)平衡常数是指可逆反应达到化学平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以该反应的平衡常数表达式为 。
。
(2)反应前氢气和碘分子的浓度都是0.01mol/L,5S时测定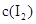 =0.0080mol/L,则消耗碘分子的浓度为0.01mol/L-0.008mol/L=0.002mol/L,生成HI是0.004mol/L,所以反应的平衡常数
=0.0080mol/L,则消耗碘分子的浓度为0.01mol/L-0.008mol/L=0.002mol/L,生成HI是0.004mol/L,所以反应的平衡常数
等于 =
=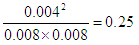
(3) 2HI(g) 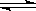 H2 + I2(g)
H2 + I2(g)
起始量(mol) 0.2 0 0
转化量(mool) 2x x x
平衡量(mol) 0.2-2x x x
逆反应的平衡常数是正反应的倒数
所以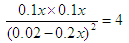
解得x=0.08
所以转化率是2x÷0.2×100%=80%
