问题
计算题
某状态下将1molO2、2molSO2和1molSO3的混合气体压入装有V2O5的密闭容器中平衡时测得混合气体对H2的相对密度为28.5。
求:①反应前混合气体的平均分子量;
②平衡混合气体的平均分子量;
③根据上述计算结果,写出原混合气发生反应的化学方程式;
④求反应的转化率。
答案
①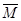 =
=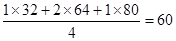
② =2×28.5=57
=2×28.5=57
③ 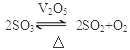
④ 2SO3  2SO2 + O2
2SO2 + O2
起始(mol): 1 2 1
转化(mol): x x 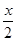
平衡(mol): 1-x 2+x. 1+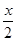
∴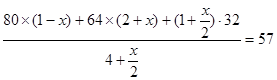
x="42.1%"
考查可逆反应的有关计算。
