(每空2分共10分)
I.在1L容器中通入CO2、H2各2mol,在一定条件下发生反应:CO2 + H2 CO + H2O,
CO + H2O,
回答下列问题:
(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。若把体系温度降至800℃求得平衡常数K1=0.81,可以推知该反应的正反应为__________反应(填“吸热”、“放热”)。
(2)800℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应 进行.(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
II.向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+2Y(s)  2Z(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
2Z(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
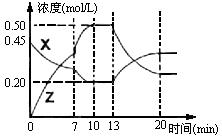
(1)0~10min 容器内气体的压强逐渐 ___________。(填“变大”、“变小”或“无法确定”)
(2)推测在第7min时曲线变化的原因可能是 ___第13min时曲线变化的原因可能是 __(填序号)
①增加Z的量 ②增加X的量 ③升温 ④降温 ⑤使用催化剂
I.(1) ① 吸热 ② 向正反应方向
II.(1)变大 (2)③⑤ (3)③
I.(1)在830℃条件下,反应达到平衡时CO2的转化率为50%,则平衡时容器内物质的物质的量都是1mol,所以此时平衡常数是1。降低温度平衡常数减小,说明降低温度平衡向逆反应方向移动,所以正反应是吸热反应。
(2)因为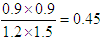 <0.81,所以向正反应方向进行。
<0.81,所以向正反应方向进行。
II.(1)根据图像可知,在0~10min时生成物的浓度增大,反应物的浓度减小,反应向正反应方向进行,即向体积增大的方向进行,所以压强增大。
(2)第7min时,物质的浓度变化程度变大,说明正逆反应速率都变大,所以答案只能是③⑤。
(3)第13min时,X的浓度增加,Z的浓度减小说明反应向逆反应方向减小。由于正反应是放热反应,所以是通过升高温度实现的。答案选③。
