已知水在25℃和95℃时,其电离平衡曲线如右图所示:
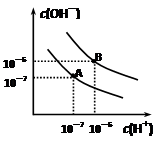
⑴则25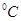 时水的电离平衡曲线应为 (填“A”或“B”)。
时水的电离平衡曲线应为 (填“A”或“B”)。
⑵25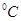 时,将
时,将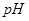 =8的NaOH溶液与
=8的NaOH溶液与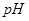 =5的
=5的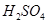 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的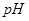 =7,则NaOH溶液与
=7,则NaOH溶液与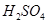 溶液的体积比为 。
溶液的体积比为 。
⑶95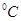 时,0.1 mol/L的NaOH溶液的pH值是 。
时,0.1 mol/L的NaOH溶液的pH值是 。
⑷95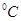 时,若100体积
时,若100体积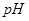 1=
1=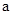 的某强酸溶液与1体积
的某强酸溶液与1体积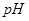 2=b的某强碱溶液混合后溶液呈中性,则混合前,
2=b的某强碱溶液混合后溶液呈中性,则混合前,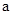 与b之间应满足的关系是
与b之间应满足的关系是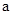 = (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
= (用含b的代数式表示),a+b_______14(填“<”、“=”或“>”)。
⑴A ⑵10:1 ⑶11 ⑷14-b,=
题目分析:(1)电离是吸热,则升高温度,电离程度增加,水中氢离子浓度增加,所以25 ℃时水的电离平衡曲线应为A。
(2)若所得混合溶液的pH=7,则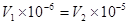 ,解得
,解得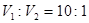 。
。
(3)95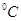 时,0.1 mol/L的NaOH溶液中OH-的浓度是0.1mol/L,则溶液中氢离子的浓度是10-11mol/L,则溶液的pH值是11。
时,0.1 mol/L的NaOH溶液中OH-的浓度是0.1mol/L,则溶液中氢离子的浓度是10-11mol/L,则溶液的pH值是11。
(4)95℃时若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则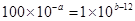 ,所以该强酸的pH1与强碱的pH2之间应满足的关系是a+b=14。
,所以该强酸的pH1与强碱的pH2之间应满足的关系是a+b=14。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生基础知识的巩固与训练,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确随着温度的升高,水的离子积常数是增大,在计算pH时需要灵活运用。
