已知N2(g)+3H2(g) 2NH3(g);ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1mol NH3。现在相同条件下的同一容器中充入xmol N2,ymol H2和2mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为
2NH3(g);ΔH=-92.4kJ/mol。在一恒温恒压的密闭容器里充入2mol N2和8mol H2达到平衡时生成1mol NH3。现在相同条件下的同一容器中充入xmol N2,ymol H2和2mol NH3,达到平衡时,NH3的质量分数与原来相同,且放出热量46.2kJ。则x、y的值为
A.5,21
B.3,13
C.2,8
D.1.5,6.5
答案:A
考查等效平衡的判断。由于是等温等压下的平衡,所以只要满足氢气和氮气的物质的量之比是4︰1即可。即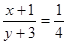 。又因为放出热量46.2kJ这说明反应中必须消耗氮气0.5mol,即生成氨气是1mol。因此平衡时容器中氨气的物质的量是3mol,所以最初氮气的物质的量是2mol×3=6mol,即x+1=6mol,所以x=5,则y=21,答案选A。
。又因为放出热量46.2kJ这说明反应中必须消耗氮气0.5mol,即生成氨气是1mol。因此平衡时容器中氨气的物质的量是3mol,所以最初氮气的物质的量是2mol×3=6mol,即x+1=6mol,所以x=5,则y=21,答案选A。
