(13分)已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素。
(1)W在周期表中的位置: 。
(2)在一定条件下,容积为1L密闭容器中加入1.2molX2和0.4molY2,发生如下反应:
3X2 (g) + Y2(g) 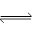 2YX3(g) △H
2YX3(g) △H
反应各物质的量浓度随时间变化如下:
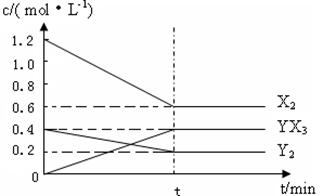
①计算该温度下此反应的平衡常数K= 。
②若升高温度平衡常数K减小,则△H 0(填“>”、“<”或“=”)。
③改变下列条件,能使该平衡向正反应方向移动且平衡常数不变的是 (填字母)。
a.增大压强 b. 降低温度 c.使用催化剂 d. 增大反应物的浓度
(3)常见液态化合物X2Z2的稀溶液易被催化分解,可使用的催化剂为 (填字母)。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)A是四种元素中三种元素组成的电解质,溶液呈碱性,将常温下0.1mol·L-1的A溶液稀释至原体积的10倍后溶液的pH=12,则A的电子式为 。
(5)以X2为燃料可制成燃料电池。已知:2X2(g)+Z2(g)=2X2Z(l) △H=−572KJ·mol-1
该燃料电池释放228.8KJ电能时,生成1mol液态X2Z,该电池的能量转化率为 。
(13分)(1)第三周期,IA(2分) (2)①K= 100/27或3.7 L2 / mol2(2分) ②<(1分) ③ad(2分) ⑶ab(2分) ⑷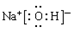 (2分) ⑸80% (2分)
(2分) ⑸80% (2分)
根据元素的性质及结构可知,X、Y、Z、W分别是H、N、O、Na。
(1)钠位于)第三周期第IA
(2)①平衡时氢气、氮气和氨气的浓度分别是0.6、0.2、0.4,所以平衡常数=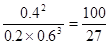 。
。
②升高温度平衡常数K减小,则平衡向逆反应方向移动,所以正反应是放热反应。
③平衡常数与温度有关系,b不正确。催化剂不能越 * * 衡状态,c不正确。增大压强或增大反应物浓度,平衡向正反应方向移动,答案选da。
(3)能使双氧水分解的是催化剂是ab。
(4)根据A的性质可知,A是强碱,所以是氢氧化钠,属于离子化合物,电子式为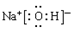 。
。
(5)生成1mol液态X2Z,放出热量是572KJ·mol-1÷2=286KJ·mol-1,属于能量转化率是228.8÷286×100%=80%。
