(14分)丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l);△H=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH="-566" kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H=
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:
CO (g)+H2O(g) CO2(g)+H2 (g)
CO2(g)+H2 (g)
①下列事实能说明该反应达到平衡的是
a.体系中的压强不发生变化 b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再发生变化
② T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:
| 时间 / min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
已知420℃时,该化学反应的平衡常数为9。如果反应开始时,CO和H2O(g)的浓度都是0.01 mol/L,则CO在此条件下的转化率为 。又知397℃时该反应的平衡常数为12,请判断该反应的△H 0 (填“>”、“=”、“<”).
(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;
燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2—。在电池内部O2—移向_ ___极(填“正”或“负”);电池的负极反应式为 。
(4)用上述燃料电池用惰性电极电解足量Mg(NO3)2和NaCl的混合溶液。电解开始后阴极的现象为____ 。
⑴-2219.9kJ/mol(2分)
(2)①bd (2分)②增加H2浓度(1分)增加H2O(g)浓度(1分) 75%(2分)△H<0(1分)
(3)负(1分) C3H8+10O2--20e-=3CO2+4H2O(2分)
(4)有大量无色气泡(或气体)产生,并且有白色沉淀产生(2分)
(1)考查盖斯定律的应用,根据已知反应可知,(①+②×3)÷2即得到C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),所以△H=(-2741.8kJ/mol-566 kJ/mol×3)÷2=-2219.9kJ/mol。
(2)①在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以d正确。反应前后体积不变,压强始终是不变的,所以a不正确。B中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确。混合气的平均相对分子质量是混合气的质量和混合气的总的物质的量的比值,质量和物质的量都是不变的,所以c不能说明。答案选bd。
②根据4min和5min浓度变化可知,CO2浓度减少,反应物浓度增加,且变化量满足化学计量数之比,所以改变的条件应该是增大氢气的浓度。根据5min和6min浓度变化可知,CO浓度减小,水蒸气浓度增大,CO2浓度增大,且CO的减少量和CO2的增加量相同,所以改变的条款是增大水蒸气的浓度。CO在此条件下的转化率为,则平衡时生成CO2和氢气分别是0.01xmol/L,因此有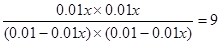 ,解得x=0.75,即转化量是75%。降低温度平衡常数增大,说明降低温度,平衡向正反应方向移动,所以正反应是放热反应。
,解得x=0.75,即转化量是75%。降低温度平衡常数增大,说明降低温度,平衡向正反应方向移动,所以正反应是放热反应。
(3)原电池中负极失去电子,所以阴离子向负极移动,丙烷在负极通入。所以负极电极反应式为C3H8+10O2--20e-=3CO2+4H2O。
(4)电解池中阴极得到电子,所以是溶液中氢离子放电,生成氢气,则同时生成OH-,所以同时液会产生氢氧化镁沉淀。
