问题
计算题
(8分)往容积为10L的密闭容器内通入40molN2和120molH2,在一定条件下进行反应,经2s后达到平衡状态,平衡时c(N2)为2mol/L。
(1)用H2的浓度变化表示2s内的平均速率为 。
(2) 氮气的转化率是 。
(3) 平衡时混合气体中氨的体积分数是 。
(4) 容器内反应前后压强比是 。
答案
(1)3mol/(L·S) (2)50% (3)33.3% (4)4∶3
考查可逆反应的有关计算,一般采用三段式。
N2 + 3H2 2NH3
2NH3
起始量(mol) 40 120 0
转化量(mol) 20 60 40
平衡量(mol) 20 60 40
(1)用H2的浓度变化表示2s内的平均速率为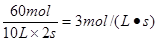
(2)氮气的转化率是20÷40×100%=50%
(3)平衡时混合气体中氨的体积分数是
(4)容器内反应前后压强比是