在80℃时,将0.8mol的A气体充入4L已抽空的固定容积的密闭容器中发生反应:A(g)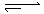 mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) c(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(A) | 0.20 | 0.14 | b | 0.09 | 0.09 | 0.09 |
| c(B) | 0.00 | 0.12 | 0.20 | c | d | e |
(2)100秒后若将容器的体积缩小至原来一半,平衡时A的浓度____________0.09 mol/L(填“<”、“=”或“>”)。
(3)在80℃时该反应的平衡常数K值为 (保留1位小数)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时 。
①A的转化率越高 ②A与B的浓度之比越大
③B的产量越大 ④正反应进行的程度越大
(8分)(1)2,< (2)> (3)0.5, (4)①②④
题目分析:(1)根据表中数据可知,反应进行到20s时,A的浓度减少了0.20mol/L-0.14mol=0.06mol/L。B的浓度增加了0.12mol/L,根据浓度的变化量之比是相应的化学计量数之比可知,m=2。根据方程式可知,(b-0.09)×2=c-0.20,解得2b=c-0.02,所以b<c。
(2)该反应是体积增大的可逆反应,所以增大压强,平衡向逆反应方向移动。则100秒后若将容器的体积缩小至原来一半,平衡时A的浓度>0.09 mol/L。
(3)根据表中数据可知,平衡时A的浓度是0.09mol/L,则平衡时B的浓度是(0.2mol/L-0.09mol/L)×2=0.22mol/L,所以在80℃时该反应的平衡常数K值为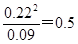 。
。
(4)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以在其他条件相同时,该反应的K值越大,则A的转化率越高,A与B的浓度之比越大,正反应进行的程度越大,但B的产量不一定越大,答案选①②④。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力,有助于提升学生的学科素养。
