问题
填空题
(12分)现有反应:CO(g)+ H2O(g) CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。
CO2(g)+ H2(g) ;△H<0。在850℃时,平衡常数K=1。
(1)若升高温度到950℃时,达到平衡时K__ ___1(填“>”、“<”或“=”)
(2)850℃时,若向一容积可变的密闭容器中同时充入 1.0 mol CO、3.0molH2O、1.0mol CO2和 x molH2,则:
①当x=5.0时,上述平衡向_______(填“正反应”或“逆反应”)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是________。
(3)在850℃时,若设x=5.0 mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a _______ b(填“>”、“<”或“=”)。
答案
(12分)(每空3分)(1) < (2) ①逆反应 ② 0≤x<3 (3) <
(1)正反应是放热反应,所以升高温度,平衡向逆反应方向移动,平衡常数减小。
(2)①当x=5.0时,此时容器中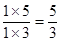 >1,所以平衡向逆反应方向移动。
>1,所以平衡向逆反应方向移动。
②若要使上述反应开始时向正反应方向进行,则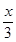 <1,即 0≤x<3 。
<1,即 0≤x<3 。
(3)如果x=5,则平衡时消耗氢气是y,所以有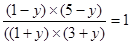 ,解得y=0.2mol,即平衡时氢气是4.8mol,其体积分数为
,解得y=0.2mol,即平衡时氢气是4.8mol,其体积分数为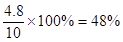 。同样如果当x=6.0mol时,可计算出平衡时氢气是52.1%,所以a小于b。
。同样如果当x=6.0mol时,可计算出平衡时氢气是52.1%,所以a小于b。