问题
实验题
(每空2分,共14分)在锌与盐酸反应的实验中,某同学得到的结果如下表所示:
| 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于水的时间/s | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
(2)利用所画的曲线图,关于温度影响反应速率的结论是 。
(3)t1 (填“>”或“<”)t4,原因是 。t2 t3(填“>”或“<”),原因是 。
答案
(每空2分,共14分)(1) 50 ,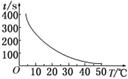
(2) 对于该溶液,温度每升高10℃,反应速率加快到原来的2倍 。
(3) > , G组中可形成Cu-Zn原电池,反应速率加快 。
> , F组中锌为粉末状,表面积较大,反应速率较快
(1)根据表中ABCD数据可知,温度每升高10℃,反应速率加快到原来的2倍,所以t1=100s÷2=5s。
(2)根据表中数据和图像可知,温度每升高10℃,反应速率加快到原来的2倍。
(3)实验G中含有杂质铜,所以能构成原电池,加快反应速率,因此时间少,即t1大于t4。又因为反应物的接触面积越大,反应速率越大,所以根据EF可知t2大于t3。
