问题
选择题
恒温(11000C)恒容密闭容器中发生反应:Na2SO4(s)+4H2(g)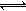 Na2S(s)+4H2O(g)
Na2S(s)+4H2O(g)
下列说法中不正确的是
A.该平衡常数表达式为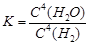
B.容器内气体的质量或压强保持不变,均可说明该反应已达到平衡状态
C.若Na2SO4足量,改变起始充入H2的浓度,则达到平衡时的H2转化率不变
D.若初始时投入2.84克Na2SO4与一定量H2,反应达到平衡时容器内固体共有2.264克,则Na2SO4的转化率为45%
答案
答案:B
根据方程式可知,反应前后气体体积是不变的,所以压强始终是不变的,选项B不正确,AC正确。根据方程式可知镁消耗142g硫酸钠,固体就减少64g,选项D中固体减少是0.576g,所以消耗的硫酸钠是1.278g,所以硫酸钠的转化率是1.278g÷2.84g×100%=45%,D正确,答案选B。