问题
选择题
下列说法正确的是
A.0.1mol氯气与足量氢氧化钠溶液(常温)反应,转移电子0.1NA
B.常温下将醋酸钠、盐酸两溶液混合后溶液呈中性,则混合溶液中: (Cl-)
(Cl-)
C.某溶液中水电离出的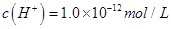 ,则此溶液中K+、
,则此溶液中K+、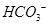 、Cl—、
、Cl—、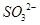 可以大量共存
可以大量共存
D.常温下物质的量浓度相等的①(NH4)2CO3溶液、②(NH4)2SO4溶液和③NH4Cl溶液中,水的电离程度:①>③>②
答案
答案:A
题目分析:Cl2与电子的对应关系为Cl2 e‾,A项正确;盐酸与醋酸钠反应生成醋酸和氯化钠,中性说明醋酸钠过量,C(Na+)>C(Cl-),B项错误;水电离出的C(H+)=1.0×10-12mol•L‾1,可能酸性也可能碱性,与HCO3‾反应,C项错误;水解程度越大,水的电离程度越大,正确顺序为:①>②>③,D项错误。
e‾,A项正确;盐酸与醋酸钠反应生成醋酸和氯化钠,中性说明醋酸钠过量,C(Na+)>C(Cl-),B项错误;水电离出的C(H+)=1.0×10-12mol•L‾1,可能酸性也可能碱性,与HCO3‾反应,C项错误;水解程度越大,水的电离程度越大,正确顺序为:①>②>③,D项错误。
