物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学的知识回答:下表是不同温度下水的离子积数据:
| 温度 / ℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-12 |
试回答下列问题:
(1)若25<t1<t2,则α________1×10-14(填“>”“<”或“=”)。
(2)25℃时,某HCl溶液中c(HCl)=1×10-4 mol·L-1,则该溶液的pH= ,此时c(H+)H2O= mol/L。加水稀释1000倍,则稀释后溶液中pH____ _7(填“>”“<”或“=”)。
(3)t2℃时,将pH=11的氢氧化钠钠溶液V1 L与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1∶V2=____________。
(1)> (2)4;1×10-10 ;< (3)9:11(2分)
题目分析:(1)水是弱电解质,存在电离平衡。而电离是吸热的,加热促进水的电离,谁的离子积常数增大。所以如果25<t1<t2,则α>1×10-14。
(2)25℃时,某HCl溶液中c(HCl)=1×10-4 mol·L-1,由于元素是强酸,完全电离,因此该溶液中氢离子浓度是1×10-4 mol·L-1,所以溶液的pH=4;此时c(H+)H2O等于溶液中OH-浓度,都等于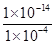 =1×10-10mol/L。加水稀释1000倍,盐酸的酸性降低,但不可能显碱性,所以则稀释后溶液中pH<7。
=1×10-10mol/L。加水稀释1000倍,盐酸的酸性降低,但不可能显碱性,所以则稀释后溶液中pH<7。
(3)t2℃时,水的离子积常数是1×10-12,此时pH=11的氢氧化钠钠溶液的浓度是0.1mol/L,V1 L该溶液与pH=1的稀硫酸V2 L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,这说明反应后硫酸是过量的,则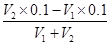 =0.01,则V1∶V2=9:11。
=0.01,则V1∶V2=9:11。
