已知任何化学反应都遵循电荷守恒和质量守恒。如下是单质铁溶于一定浓度的硝酸中反应的化学方程式:
aFe+b +cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)
+cH+====dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数均为正整数)
请你用已掌握的知识研究出下列规律:
(1)c、g、h的关系式是___________________;
(2)b、c、d、f的关系式是________________;
(3)d、f、g、h的关系式是______________。
c="4g+10h " c-b="2d+3f " 2d+3f=3g+8h
(1)这是考查反应前后H、O原子守恒关系。若只从“cH+ gNO+hN2O”去分析,似乎H+跟NO、N2O之间没有什么联系,思路不容易展开。只要抓住“反应中H+全部转化为H2O”“NO和N2O全是由
gNO+hN2O”去分析,似乎H+跟NO、N2O之间没有什么联系,思路不容易展开。只要抓住“反应中H+全部转化为H2O”“NO和N2O全是由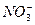 转变而来”,必有“
转变而来”,必有“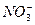
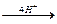 NO+2H2O”和“2
NO+2H2O”和“2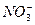
 N2O+5H2O”,进而总结出“c=4g+10h”。
N2O+5H2O”,进而总结出“c=4g+10h”。
(2)这是考查电荷守恒关系。离子反应中反应物微粒所带的电荷数和生成物微粒所带的电荷数必定相等。b、c、d、f恰好是反应方程式中各种离子的化学计量数,因此根据“b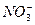 +cH+
+cH+ dFe2++fFe3+”就可计算出“c-b=2d+3f”。
dFe2++fFe3+”就可计算出“c-b=2d+3f”。
(3)这是考查电子守恒关系。d、f、g、h恰好是与电子得失有关四种产物的化学计量数,其中“dFe2++fFe3+”决定失电子总数,“gNO+hN2O”决定得电子总数,所以有“2d+3f====3g+8h”。