(13分)在25℃时,将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g) 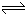 xC(g)+2D(g) ;△H>0,经5min后测知D的浓度为0.5mol/L,
xC(g)+2D(g) ;△H>0,经5min后测知D的浓度为0.5mol/L,
A、B的物质的量浓度之比为3:5,C的平均反应速率是0.1mol/(L·min),求:
(1)此时A的物质的量浓度是 ;
反应开始前容器中的A、B的物质的量:n(A)= n(B)=
(2)x的值为 ;5min内B的平均反应速率 ;
(3)下列措施能使正反应速率增大的是 (不定项选择)
A. 只增大A的浓度 B.增大反应的温度
C. 向容器中通入一定体积的He,增大反应的压强 D. 使用催化剂
(4)若改用3L的密闭容器,盛放与上述相同量的A、B气体,则达到平衡后,A和B的物质的量浓度的比值 3:5(填“>”“=”“<”)。
(13分)(1)0.75mol/L 3mol (2)0.05mol/(L·min) 2
(3) ABD (4)=
考查可逆反应的有关计算及外界条件对反应速率和平衡的影响。
(1)C的平均反应速率是0.1mol/(L·min),则C的浓度是0.5mol/L,所以根据变化量之比是相应的化学计量数之比可知x=2。又因为反应速率之比是相应的化学计量数之比,所以B的反应速率是0.1mol/(L·min)÷2=0.05mol/(L·min)。
(2) 3A(g)+B(g) 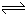 2C(g)+2D(g)
2C(g)+2D(g)
起始量(mol) n n 0 0
转化量(mol) 1.5 0.5 1.0 1.0
平衡量(mol) n-1.5 n-0.5 1.0 1.0
所以有(n-1.5)︰(n-0.5)= 3:5
解得n=3mol,所以A的浓度是1.5mol÷2L=0.75mol/L
(3)在其它条件不变的情况下,增大反应物浓度或升高温度或增大压强或使用催化剂等均能加快反应速率,选项C中浓度不变,反应速率不变,所以答案选ABD。
(4)因为反应前后体积不变,所以此时的平衡是等效的,因此比值不变。
