问题
选择题
将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应: H2NCOONH4(s)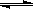 2NH3(g)+CO2(g)。在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
2NH3(g)+CO2(g)。在不同温度下,该反应平衡状态部分数据见右表。下列说法正确的是
| 平衡浓度/ (mol L-1) | ||
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | 0.1 | |
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,H2NCOONH4转化的物质的量:Δn(T2)=2Δn(T1)
答案
根据方程式可知,T1时CO2的浓度是0.05mol/L。而在T2时,CO2的浓度是0.1mol/L,这说明若T2>T1,即升高温度平衡向正反应方向移动,所以正反应是吸热反应,△H大于0,A不正确;氮气不参与反应,充入氮气平衡不移动,B不正确;由于氨气和CO2的体积之比总是2︰1的,所以氨气的体积分数始终是不变的,C不正确;T2时CO2的浓度是T1时CO2的2倍,所以T2时反应物的转化率是T1时的2倍,D正确,答案选D。
