某学生用0.10 mol/L标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
| 实验序号 | 待测液体积(mL) | 所消耗NaOH标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.54 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.36 |
(1)滴定时选用酚酞试液作指示剂,如何判断滴定达到终点 。
(2)盐酸的物质的量浓度为_____________
(3)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是 (填“偏高”或“偏低”或“无影响”,下同)。
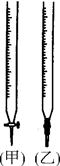
(4)某同学用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,高锰酸钾溶液应盛放在 中(填“甲”或“乙”),该反应的离子方程式为: 。
(1)当滴入最后一滴标准液,溶液由无色变为浅红色,且半分钟内不退色
(2)0.10mol/L (3) 偏高(4) 甲 5Fe2+ + MnO4- + 8H+ = 5Fe2+ + Mn2+ + 4H2O
题目分析:(1)因为这是由已知浓度的碱滴定未知浓度的酸,酚酞指示剂在酸溶液中,是无色的,随着碱的滴加,溶液的酸性逐渐减弱,当滴加到最后一滴时,溶液由无色变为浅红色,半分钟内不褪色时酸碱中和恰好完成。(2)碱溶液的平均体积为V=(V1+V2+V3)÷3=" ((20.54-0.05)+(26.00-6.00)" +(21.36-1.40)) ÷3=20.00ml,利用酸碱恰好发生中和反应时C酸••V酸=C碱•V碱,C酸="(" C碱•V碱) ÷V酸="(0.10" mol/L×20.00ml) ÷20.00ml="0.10mol/L." (3)若在滴定前碱式滴定管尖嘴部分有气泡,滴定后消失,碱溶液的体积偏大,以此为标准计算的酸的浓度偏高。(4)若用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,由于高锰酸钾溶液有强的氧化性,容易腐蚀碱式滴定管的橡胶管,所以应盛放在酸式滴定管甲中,发生该反应的离子方程式为5Fe2+ + MnO4- + 8H+ = 5Fe2+ + Mn2+ + 4H2O。
