问题
选择题
下列有关溶液中粒子浓度的关系式中,正确的是( )
A.pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中: c(Na+)=2c(A2-)+c(HA-)+c(H2A)
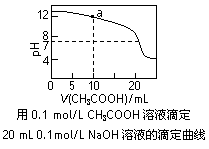
C.图中pH=7时:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D.图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
答案
答案:D
题目分析:A.已知酸性:醋酸>碳酸>碳酸氢钠,酸性越强,对应的盐水解程度越大,当pH相同时,浓度:①>②>③,故A错误;B.NaHA溶液中存在物料守恒:c(Na+)=c(A2﹣)+c(HA﹣)+c(H2A),故B错误;C.图中pH=7时,c(OH﹣)=c(H+),因c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣),则c(Na+)=c(CH3COO﹣),故C错误;D.a点溶液溶质为NaOH和CH3COONa,溶液中存在电荷守恒:c(CH3COO﹣)+c(OH﹣)=c(H+)+c(Na+),物料守恒:c(Na+)=2c(CH3COO﹣)+2c(CH3COOH),二者联式可得:c(OH﹣)=c(H+)+c(CH3COO﹣)+2c(CH3COOH),故D正确,故选D.
