(共16分)
(1)现有反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
①该反应的逆反应为______反应(填“吸热”或“放热”),且m+n______ p (填“>”、“=”或“<”)。
②减压使容器体积增大时,A的质量分数________。(填“增大”、“减小”或“不变”,下同)
③若容积不变加入B,则A的转化率__________,B的转化率________。
④若升高温度,则平衡时B、C的浓度之比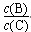 将________。
将________。
⑤若加入催化剂,平衡时气体混合物的总物质的量________________________________
(2)在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应:
N2(g)+3H2(g) 2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:
2NH3(g) ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示,请回答下列问题:
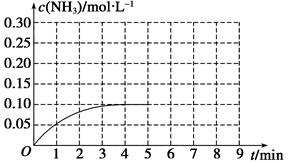
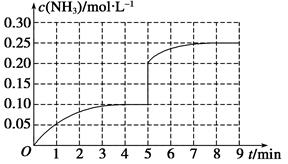
在第5 min末将容器的体积缩小一半后,若在第8 min末达到新的平衡(此时NH3的浓度约为0.25 mol·L-1),请在图中画出第5 min末到平衡时NH3浓度的变化曲线。
(1)①放热 > ②增大 ③增大 减小 ④减小 ⑤不变
(2)如图
(1)反应:mA(g)+nB(g)  pC(g),达到平衡后,当升高温度时,B的转化率变大,说明正向移动,为吸热反应;当减小压强时,混合体系中C的质量分数减小,则平衡左移,正反应的气体系数减小。则:
pC(g),达到平衡后,当升高温度时,B的转化率变大,说明正向移动,为吸热反应;当减小压强时,混合体系中C的质量分数减小,则平衡左移,正反应的气体系数减小。则:
②减压平衡逆向移动,A的质量分数增大
③若容积不变加入B,平衡右移,则A的转化率增大,而B的转化率减小。
④升高温度,则平衡正向移动,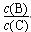 将减小。
将减小。
⑤若加入催化剂,平衡不受影响,气体混合物的总物质的量不变
(2)_ N2(g) + 3H2(g)  2NH3(g)
2NH3(g)
初c: 0.1 0.3 0
5min时c: 0.05 0.15 0.1
此时缩小容器体积一半,各物质浓度同倍数增大一倍,相当于增压,平衡正向移动。
_ N2(g) + 3H2(g)  2NH3(g)
2NH3(g)
5min时c: 0.1 0.3 0.2
8 min时c: 0.25
