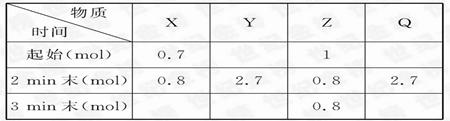
(16分).在2 L密闭容器中进行反应:mX(g)+nY(g) 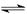 pZ(g)+qQ(g),式中m、n、p、q为物质系数。在0 min~3 min 内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为物质系数。在0 min~3 min 内,各物质物质的量的变化如下表所示:
已知2 min内 v(Q)="0.075" mol·L-1·min-1,且 v(z):v(Y)=1:2
(1)试确定以下物质的相关量:起始时n(Y)=________,n(Q)=_________。
(2)方程式中m =______,n =______,p=______,q=_______。
(3)用Z表示2 min内的反应速率_____________。
(4)2 min末Q的转化率为_____________
(5)试判断在2 min内v(正)______v(逆)(填“>”、“<”或“=”),在2 min末~3 min末v(正)_____ v(逆)(填“>”、“<”或“=”)。
(共16分,第2小题每空1分,其余每空2分)
(1)2.3 mol 3 mol (2)1 4 2 3
(3)0.05 mol·L-1·min-1 (4)10% (5)< =
题目分析:(1)根据表中数据可知,2min末Z物质的浓度不再发生变化,所以反应到达平衡状态。根据v(Q)="0.075" mol·L-1·min-1可知,Q物质的变化量是0.075 mol·L-1·min-1×2L×2min=0.3mol,所以Q的起始量是0.3mol+2.7mol=3.0mol。Z物质的变化量是0.2mol,所以p=2、q=3,则n=4。又因为X的变化量是0.1mol,所以m=1。生成Y物质的物质的量是0.1mol×4=0.4mol,所以Y的起始量是2.7mol-0.4mol=2.3mol。
(2)见(1)中分析
(3)Z物质的变化量是0.2mol,所以用Z表示2 min内的反应速率是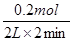 =0.05 mol·L-1·min-1。
=0.05 mol·L-1·min-1。
(4)2 min末Q的转化率是0.3÷3.0×100%=10%。
(5)在2 min内该反应没有达到平衡状态,但由于是从生成物开始建立平衡的,所以v(正)小于v(逆)。2min时反应达到平衡状态,所以v(正)等于v(逆)。
点评:在进行反应速率的有关计算时,必须要利用反应速率之比是相应的化学计量数之比这一关系式进行有关的计算和判断。