问题
选择题
常温下,向0.1 mol/L的H2SO4溶液中逐滴加入0.1 mol/L的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示,下列说法中正确的是
( )
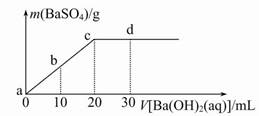
A.a~d溶液的pH:a<b<c<d
B.a~d溶液的导电能力:a<b<c<d
C.b处溶液的c(H+)与d处溶液的c (OH-)相等
D.c处溶液和d处溶液均呈碱性
答案
答案:A
A项,0.1 mol/L的H2SO4溶液呈酸性,不断地加入Ba(OH)2溶液,碱性会不断增强,故A正确;B项,c点是H2SO4和Ba(OH)2恰好中和的点,溶液的离子浓度接近为0,导电能力最差,故B错误;C项,由图像可知,原硫酸体积为20 mL,b处溶液的c(H+)=[0.1 mol/L×2×0.02-0.1 mol/L×2×0.01]/
0.03 L, d处溶液的c(OH-)= [0.1 mol/L×2×0.03-0.1 mol/L×2×0.02]/0.05,b处溶液的c(H+)不等于d处溶液的c(OH-),故C错误;D项,c处溶液呈中性,D错误
