已知某化学反应的平衡常数表达式为K= ,在不同的温度下该反应的平衡常数值分别为:
,在不同的温度下该反应的平衡常数值分别为:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
A.该反应的化学方程式是:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830 ℃,此时测得CO为0.4 mol时,该反应为平衡状态
D.某温度下,如果平衡浓度符合下列关系式: ,判断此时的温度是1000 ℃
,判断此时的温度是1000 ℃
答案:C
题目分析:化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以关键平衡常数的表达式可知,反应的化学方程式是CO(g)+H2O(g) CO2(g)+H2(g),A正确;随着温度的升高,平衡常数是减小的,这说明升高温度平衡向逆反应方向进行,所以正反应是放热反应,B正确;CO为0.4 mol,则水蒸气也是0.4mol,CO2和氢气都是0.6mol,则此时
CO2(g)+H2(g),A正确;随着温度的升高,平衡常数是减小的,这说明升高温度平衡向逆反应方向进行,所以正反应是放热反应,B正确;CO为0.4 mol,则水蒸气也是0.4mol,CO2和氢气都是0.6mol,则此时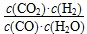 =
=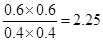 >1.00,所以没有达到平衡状态,C不正确;将
>1.00,所以没有达到平衡状态,C不正确;将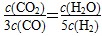 带入平衡常数表达式可得K=0.6,所以温度是1000℃,D正确,答案选C。
带入平衡常数表达式可得K=0.6,所以温度是1000℃,D正确,答案选C。
点评:在判断外界条件对平衡状态的影响时,应该利用勒夏特列原理进行。
