问题
选择题
恒温恒容的三个密闭容器,N2(g)+3H2(g)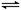 2NH3(g) △H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表。下列叙述正确的是
2NH3(g) △H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表。下列叙述正确的是
| 容器 编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
B.三个容器内反应的平衡常数③>①>②
C.N2的转化率①<②
D.达平衡时氨气的体积分数①>③
答案
答案:A
题目分析:根据表中数据可知,②相当于是在①的基础上增大氮气的浓度,平衡向正反应方向进行,氢气的转化率增大,A正确。但氮气的转化率降低,C不正确;温度相同,平衡常数不变,B不正确;③和①相比,相当于是在①的基础上增大压强,平衡向正反应方向移动,氨气的体积分数增大,D不正确,答案选A。
点评:在判断①和③时可以利用等效平衡进行。所谓等效平衡是指外界条件相同时,同一可逆反应只要起始浓度相当,无论经过何种途径,都可以达到相同的平衡状态。等效平衡的判断及处理一般步骤是:进行等效转化——边倒法,即按照反应方程式的计量数之比转化到同一边的量,与题干所给起始投料情况比较。恒温恒容下对于反应前后气体体积发生变化的反应来说(即△n≠0的体系):等效转化后,对应各物质起始投料的物质的量与原平衡起始态相同。显然该题中①和③的平衡是不等效的,所以需要把③中反应物的均分2份,然后在压缩即可与①进行对比。
