在a mL醋酸溶液中滴加0.01 mol·L-1的氢氧化钠溶液,滴定曲线如图所示。
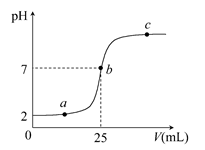
(1)醋酸溶液浓度________(填“大于”“小于”或“等于”)0.01 mol·L-1,理由是________;
(2)b点,c(Na+)________c(CH3COO-)(填“>”“<”或“=”)
(3)当醋酸与氢氧化钠溶液恰好完全中和时,曲线上对应的点Q应在____;
A.2与a之间 B.a与b之间
C.b与c之间 D.a与c之间
(4)下列关系式一定正确的是________。
A.a点,c(H+)>c(OH-)>c(CH3COO-)>c(Na+)
B.a点,c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.c点,c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c点,c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
(1)大于;CH3COOH是弱电解质,只部分电离
(2)= (3)C (4)D
(1)开始时,醋酸溶液的pH=2,c(H+)=0.01 mol·L-1,由于醋酸是弱电解质,醋酸溶液中存在未电离的CH3COOH,故c(CH3COOH)>0.01 mol·L-1。(2)b点,pH=7表示c(H+)=c(OH-),由电荷守恒式c(Na+)+c(H+)=c(OH-)+c(CH3COO-)得出:c(Na+)=c(CH3COO-)。(3)CH3COOH+NaOH=CH3COONa+H2O,当醋酸与氢氧化钠恰好完全中和时,溶液呈碱性,pH>7,曲线上对应的Q点应在b与c之间。(4)a点,溶液的溶质是醋酸和醋酸钠,溶液显酸性,醋酸是弱酸,离子浓度大小关系为:c(CH3COO-)>c(H+)>c(OH-);无论溶液呈酸性、中性或碱性,其中都只存在Na+、H+、CH3COO-、OH-,所以一定有电荷守恒式,D选项正确。
