问题
选择题
某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25°C
B.由水电离出来的H+的浓度是1.0×10-10 mol/L
C.加入NaHSO4晶体抑制了水的电离
D.该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性
答案
答案:D
某温度下蒸馏水的pH=6,所以KW=1.0×10-12,25°C时的KW=1.0×10-14,所以温度高于25°C,A正确。c(H+)水=c(OH-)水=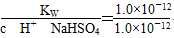 =1.0×10-10(mol/L),故B正确;NaHSO4能完全电离出氢离子,相当于一元强酸,抑制水的电离,C正确。注意KW=1.0×10-12,所以应加入等体积pH=10的NaOH溶液,才能使该溶液恰好呈中性,所以D错误。
=1.0×10-10(mol/L),故B正确;NaHSO4能完全电离出氢离子,相当于一元强酸,抑制水的电离,C正确。注意KW=1.0×10-12,所以应加入等体积pH=10的NaOH溶液,才能使该溶液恰好呈中性,所以D错误。
