高氯酸铵样品中 NH4ClO4的含量可用蒸馏法进行测定,蒸馏装置如图所示(加热和仪器固定装置已略去),实验步骤如下:
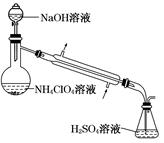
步骤 1:按如图所示组装仪器,检查装置气密性。
步骤 2:准确称取样品a g (约 0.5 g)于蒸馏烧瓶中,加入约 150 mL 水溶解。
步骤 3:准确量取 40.00 mL 约 0.1 mol·L-1 H2SO4溶液于锥形瓶中。
步骤 4:经滴液漏斗向蒸馏烧瓶中加入 20 mL 3 mol·L-1NaOH 溶液。
步骤 5:加热蒸馏至蒸馏烧瓶中剩余约 100 mL 溶液。
步骤 6:用新煮沸过的水冲洗冷凝装置 2~3 次,洗涤液并入锥形瓶中。
步骤 7:向锥形瓶中加入酸碱指示剂,用 c mol·L-1NaOH 标准溶液滴定至终点,消耗 NaOH 标准溶液 V1 mL。
步骤 8:将实验步骤 1~7 重复 2 次。
①步骤 3中,准确量取 40.00 mL H2SO4溶液的玻璃仪器是 。
②步骤 1~7 中,确保生成的氨被稀硫酸完全吸收的实验步骤是 (填步骤序号)。
③为获得样品中 NH4ClO4的含量,还需补充的实验是 。
①酸式滴定管
②1,5,6
③用NaOH标准溶液标定H2SO4溶液的浓度(或不加高氯酸铵样品,保持其他条件相同,进行蒸馏和滴定实验)
①准确量取40.00 mL H2SO4溶液可以选用量程为50 mL的酸式滴定管。③本实验采用高氯酸铵与氢氧化钠溶液反应,生成的氨气与过量的稀硫酸反应,再用已知浓度的氢氧化钠溶液滴定剩余的硫酸,从而计算出产生的氨气的物质的量,进一步换算出样品中高氯酸铵的含量。因步骤3中所给H2SO4的浓度值非精确值,故为了提高实验结果的准确度,还应该用氢氧化钠标准溶液标定硫酸的浓度。
