问题
选择题
通常人们把拆开1 mol某化学键所吸收的能量或形成1 mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知
| 化学健 | H-H | Cl-Cl | H-Cl |
| 键能 | 436 kJ·mol-1 | 243 kJ·mol-1 | 431 kJ·mol-1 |
则下列热化学方程式不正确的是( )
A.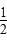 H2(g)+
H2(g)+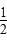 Cl2(g)=HCl(g)ΔH=-91.5 kJ·mol-1
Cl2(g)=HCl(g)ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g)ΔH=-183 kJ·mol-1
C.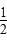 H2(g)+
H2(g)+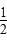 Cl2(g)=HCl(g)ΔH=91.5 kJ·mol-1
Cl2(g)=HCl(g)ΔH=91.5 kJ·mol-1
D.2HCl(g)=H2(g)+Cl2(g)ΔH=183 kJ·mol-1
答案
答案:C
化学反应的实质是旧键断裂,新键生成,断键吸热,成键放热,根据各化学
键的键能可知H2和Cl2的反应是放热反应,C错误,A、B、D中ΔH的数据与化
学方程式中的系数关系是正确的。
