问题
选择题
在25℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(l)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为( )
A.-488.3 kJ/mol
B.+488.3 kJ/mol
C.-191 kJ/mol
D.+191 kJ/mol
答案
答案:A
由题意可知:C(s)+O2(g)=CO2(g)ΔH=-393.5 kJ/mol ①
H2(g)+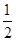 O2(g)=H2O(l)ΔH=-285.8 kJ/mol ②
O2(g)=H2O(l)ΔH=-285.8 kJ/mol ②
CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)ΔH=-870.3 kJ/mol ③
①×2+②×2-③即得:
2C(s)+2H2(g)+O2(g)=CH3COOH(l)ΔH=-488.3 kJ/mol。
