(14分)“氢能”将是未来最理想的新能源。
Ⅰ 在25℃,101KPa条件下,1 g氢气完全燃烧生成液态水时放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为 。
Ⅱ 氢气通常用生产水煤气的方法制得。其中CO(g)+ H2O(g) CO2(g)+H2(g) △H<0。在850℃时,平衡常数K=1。
CO2(g)+H2(g) △H<0。在850℃时,平衡常数K=1。
(1)若升高温度至950℃,达到新平衡状态时K (填“>”、“<”或“=”)1。
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0 molCO、3.0mol H2O、1.0 molCO2和x mol H2,则:
①当x = 5.0时,上述平衡向 (填“正反应”或“逆反应”)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是 。
③若设x="5.0" mol和x="6.0" mol,其他物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a (填“>”、“<”或“=”)b。
Ⅲ 海水淡化获得淡水的过程也可以产生氢气。下面是利用电渗析法处理海水获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:
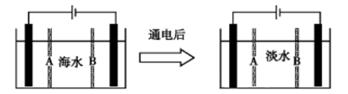
(1)阳离子交换膜是指______________ (填A或B)。
(2)写出通电后阳极的电极反应式:_________________________________________,在阴极区观察到的现象是:_________________________________________。
ⅠH2(g)+ 1/2O2(g)=H2O(l) △H=-285.8kJ/mol(2分)
Ⅱ(1)<(1分)(2) ①逆反应(2分)②0≤x<3或x<3(2分)③<(2分)
Ⅲ (1)B(1分) (2)2Cl--2e-═Cl2↑;出现白色沉淀
题目分析:Ⅰ 在25℃,101KPa条件下,1 g氢气完全燃烧生成液态水时放出142.9kJ热量,则2g氢气即1mol氢气完全燃烧生成液态水时放出142.9kJ热量×2=285.8kJ。由于燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,则表示氢气燃烧热的热化学方程式为H2(g)+ 1/2O2(g)=H2O(l) △H=-285.8kJ/mol。
Ⅱ(1)正方应是放热反应,因此升高温度平衡向逆反应方向进行,则若升高温度至950℃,达到新平衡状态时K<1。
(2)①由于反应前后体积不变,则可以用物质的量表示浓度计算平衡常数。则当x = 5.0时,此时浓度商为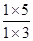 >1,因此反应向逆反应方向进行。
>1,因此反应向逆反应方向进行。
②若要使上述反应开始时向正反应方向进行,则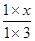 <1,解得x<3,因此x应满足的条件是0≤x<3。
<1,解得x<3,因此x应满足的条件是0≤x<3。
③增大一种生成物(氢气)的体积分数,平衡向逆反应方向移动,平衡移动的结果是降低这种增大的幅度,故平衡后氢气的体积分数还是大于原来的。
Ⅲ(1)阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过,隔膜B和阴极相连,阴极是阳离子放电,所以隔膜B是阳离子交换膜。
(2)根据阳极是氯离子放电:2Cl--2e-═Cl2↑,阴极区是氢离子得到电子生成氢气,氢氧根离子浓度增大,和钙离子,镁离子形成沉淀。
