(12分,每空2分)一定的条件下,在某一容积为2L的密闭容器内,物质A、B、C发生某种放热化学反应,反应中物质A、B、C的浓度随时间变化情况如图1:
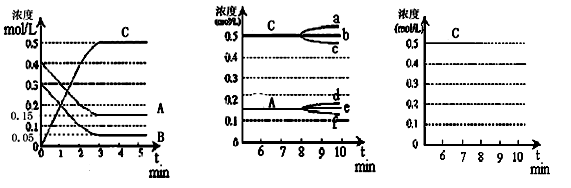
(1)该反应化学方程式为_____________________________________,该反应的逆反应化学平衡常数表达式为___________;
(2)根据图1数据,反应开始至达到平衡时,平均速率v(C)为________________;
(3)反应达到平衡后,第8分钟时:
①若升高温度,C浓度的变化正确________;(用图2中a~f的编号回答)
②若加入B,该反应的平衡常数将____________。(填“增大”或“不变”或“减小”)
(4)反应达到平衡后,第8分钟时,若反应容器的容积扩大一倍,请在图3中用“粗线条”画出8分钟后C浓度的变化情况。
(每空2分,总计12分)
(1)A + B  2C;
2C; 
(2)0.167mol/(L•min)或0.17mol/(L•min);
(3)① c; ② 不变。
(4)
题目分析:(1)开始反应时反应物的浓度减少,生成物的浓度增大,最后浓度都不再变化,故A、B是反应物,C是生成物,根据化学计量数之比只与反应的物质的量之比,因此,反应方程式为:A + B  2C。化学平衡常熟等于反应物的浓度幂之积除以生成物的浓度幂之积的值,故逆反应化学平衡常数表达式为
2C。化学平衡常熟等于反应物的浓度幂之积除以生成物的浓度幂之积的值,故逆反应化学平衡常数表达式为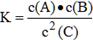 。
。
(2)根据公式计算,v(C)=∆ c(C)/∆t=0.5(mol/L)/3min=0.167mol/(L•min)。
(3)①升高温度,化学平衡逆向移动,C的浓度会减少,故c图像是正确的。
②平衡常数只与温度有关,故平衡常数不变。
(4)反应是前后气体体积不变的反应,改变容器的体积(气体的压强),化学平衡不移动,体积扩大一倍,物质的浓度都减少一半。
点评:本题考查了反应速率、平衡常数计算和平衡移动,难度适中,注意化学平衡常数与温度有关。
