300℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:
3A(g)+B(g)  2C(g)+2D(g);ΔH=Q,2 min末达到平衡,生成0.8 mol D.
2C(g)+2D(g);ΔH=Q,2 min末达到平衡,生成0.8 mol D.
(1)300℃时,该反应的平衡常数表达式为:K=___________.
已知K300℃<K350℃,则ΔH________0(填“>”或“<”).
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为______________.
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”、“减小”或“不变”),原因是__________________________________________________.
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时若加入C、D各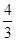 mol.若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________ mol.
mol.若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________ mol.
(共10分,前4空每空各1分,其余每空2分)
(1)K=c2(C)·c2(D)/ c3(A) ·c (B) >
(2) 0.8 mol·L-1 0.2 mol·L-1·min-1
(3)不变 反应前后气体体积不变,压强对平衡无影响 (4) 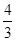
题目分析:(1) 化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的化学方程式可知,300℃时,该反应的平衡常数表达式为K=c2(C)·c2(D)/ c3(A) ·c (B)。如果K300℃<K350℃,这说明升高温度,平衡向正反应方向移动,则ΔH>0。
(2) 3A(g)+B(g)  2C(g)+2D(g)
2C(g)+2D(g)
起始浓度(mol/L) 1 1 0 0
转化浓度(mol/L) 0.6 0.2 0.4 0.4
平衡浓度(mol/L) 0.4 0.8 0.4 0.4
所以D的平均反应速率为0.4mol/L÷2min=0.2 mol·L-1·min-1
(3)反应前后气体体积不变,压强对平衡无影响,所以若温度不变,缩小容器容积,则A的转化率不变。
(4)如果在相同的条件下,上述反应从逆反应方向进行,则把C、D的量转化为A和B之和应该和最初A、B的物质的量相等。C、D各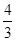 mol完全转化为A是2mol,B是
mol完全转化为A是2mol,B是 ,所以还应该加入B是2mol-
,所以还应该加入B是2mol- =
= 。
。
点评:该题是中等难度的试题,也是高考中的常见题型。试题基础性强,难易适中。在注重对学生基础性知识巩固和训练的同时,侧重对学生解题方法和能力的培养,有助于培养学生的逻辑推理能力,提高学生的应试能力。该题的难点是等效平衡的判断和有关计算。
