二甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效,具有优良的环保性能。也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。请填写下列空白:
(1)二甲醚的核磁共振H谱图中有____________个吸收峰,官能团名称是____________ 。
(2)二甲醚、空气、氢氧化钾溶液、多孔石墨电极可构成燃料电池。该电池中负极的电极反应式是:
CH3OCH3+16OH- -12e- = 2CO32- +11H2O,则正极的电极反应式是___________________________。
(3)利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g) 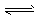 CH3OH(g) ΔH=a kJ·mol-1
CH3OH(g) ΔH=a kJ·mol-1
② 2CH3OH(g) 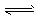 CH3OCH3(g) + H2O(g) ΔH=b kJ·mol-1
CH3OCH3(g) + H2O(g) ΔH=b kJ·mol-1
③ CO(g) + H2O(g)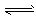 CO2(g) + H2(g) ΔH=ckJ·mol-1
CO2(g) + H2(g) ΔH=ckJ·mol-1
总反应:3H2(g) + 3CO(g) 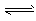 CH3OCH3(g) + CO2 (g)的ΔH= __________ kJ·mol-1。
CH3OCH3(g) + CO2 (g)的ΔH= __________ kJ·mol-1。
(4) 已知反应②2CH3OH(g) 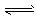 CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下

①比较此时正、逆反应速率的大小:v(正) ______ v(逆)(填“>”、“<”或“=”),因为该时刻的浓度商QC 平衡常数_________400(填“>”、“<”或“=”)。
② 若开始只加入CH3OH,经10min后反应达到平衡,平衡时CH3OH转化率α (CH3OH) ____________(计算结果用百分数表示,保留小数后一位)。
(1)1 ;醚键
(2) 6H2O+3O2+12e- = 12OH-或:2H2O+O2+4e- = 4OH-
(3) 2a+b+c
(4) ①> ;< ;②97.6%
