化学反应原理在科研和生产中有广泛应用
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应TaS2(s)+2I2(g) TaI4(g)+S2(g) △H﹥0 (Ⅰ)反应(Ⅰ)的平衡常数表达式K= ,若K=1,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为 ,
TaI4(g)+S2(g) △H﹥0 (Ⅰ)反应(Ⅰ)的平衡常数表达式K= ,若K=1,向某恒容密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为 ,
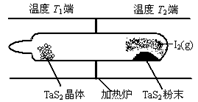
(2)如图所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净的TaS2晶体,则温度T1 T2(填“﹥”“﹤”或“=”)。上述反应体系中循环使用的物质是 。
(3)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化为 H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为 ,滴定反应的离子方程式为 ,
(4)25℃时,H2SO3 HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh= mol/L,若向NaHSO3溶液中加入少量的I2,则溶液中
HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh= mol/L,若向NaHSO3溶液中加入少量的I2,则溶液中 将 (填“增大”“减小”或“不变”)。
将 (填“增大”“减小”或“不变”)。
(1)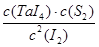 ;66.7%;
;66.7%;
(2)<; I2;
(3)淀粉; H2SO3+I2+H2O=2I-+SO42-+4H+;
(4)1.0×10-12;增大。
(1)根据题给的化学方程式:TaS2(s)+2I2(g) TaI4(g)+S2(g),可知K=
TaI4(g)+S2(g),可知K=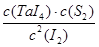 ;由于K=1,设平衡时TaI4和S2的物质的量为x,则根据平衡常数可列式:(x/V)2=【(1-2x)/V】2,即:x2=(1-2x)2,解得x=1/3,故I2(g)的平衡转化率为:(2/3)×100%=66.7%;
;由于K=1,设平衡时TaI4和S2的物质的量为x,则根据平衡常数可列式:(x/V)2=【(1-2x)/V】2,即:x2=(1-2x)2,解得x=1/3,故I2(g)的平衡转化率为:(2/3)×100%=66.7%;
(2)分析题给的化学方程式:TaS2(s)+2I2(g) TaI4(g)+S2(g) △H﹥0,该反应正向吸热;由于反应先在T2端开始,一段时间后在T1端得到晶体,说明反应生成的气体在T1端温度降低平衡左移,故温度T1<T2;在上述变化过程中I2可以循环使用;
TaI4(g)+S2(g) △H﹥0,该反应正向吸热;由于反应先在T2端开始,一段时间后在T1端得到晶体,说明反应生成的气体在T1端温度降低平衡左移,故温度T1<T2;在上述变化过程中I2可以循环使用;
(3)利用I2的氧化性可测定钢铁中硫的含量时的指示剂是淀粉,反应的离子方程式为:H2SO3+I2+H2O= 2I-+SO42-+4H+;
(4)根据NaHSO3的水解方程式:HSO3-+H2O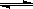 H2SO3+OH-,其水解平衡常数的表达式为:Kh=c(H2SO3)×c(OH-)/c(HSO3-),故Ka×Kh= c(H+)×c(OH-)=Kw,可求出Kh =1.0×10-12;若向NaHSO3溶液中加入少量的I2,溶液中发生反应:HSO32-+I2+H2O=SO42-+2I-+3H+,氢离子结合氢氧根离子,使平衡向右移动,造成溶液中
H2SO3+OH-,其水解平衡常数的表达式为:Kh=c(H2SO3)×c(OH-)/c(HSO3-),故Ka×Kh= c(H+)×c(OH-)=Kw,可求出Kh =1.0×10-12;若向NaHSO3溶液中加入少量的I2,溶液中发生反应:HSO32-+I2+H2O=SO42-+2I-+3H+,氢离子结合氢氧根离子,使平衡向右移动,造成溶液中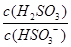 增大。
增大。
【考点定位】此题综合考查了化学平衡常数、电离平衡常数和水解平衡常数、平衡转化率、化学平衡的移动、滴定指示剂的选择等知识。
