问题
填空题
已知:2SO2(g)+O2(g)
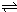
2SO3(g)△H=-196.6kJ•mol-1
2NO(g)+O2(g)
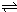
2NO2(g)△H=-113.0kJ•mol-1
写出NO2(g)与SO2(g)生成SO3(g)和NO(g)热化学方程式______.
(2)已知N2与H2反应生成NH3的能量变化如图所示:
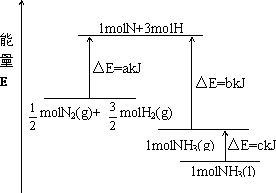
则
N2(g)+1 2
H2(g)3 2
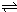
NH3(l);△H=______.
答案
(1)由①2SO2(g)+O2(g)
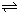
2SO3(g)△H=-196.6kJ•mol-1,
②2NO(g)+O2(g)
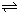
2NO2(g)△H=-113.0kJ•mol-1,
根据盖斯定律可知,
可得NO2(g)+SO2(g)═SO3(g)+NO(g),①-② 2
则△H=
=-41.8kJ•mol-1,-196.6kJ/mol-(-113.0kJ/mol) 2
故答案为:NO2(g)+SO2(g)═SO3(g)+NO(g)△H=-41.8kJ•mol-1;
(2)由图可知,生成1molNH3(g)放出的热量为b-akJ,由气体变为液体,放出热量为ckJ,
则
N2(g)+1 2
H2(g)3 2
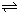
NH3(l)△H=-(b-a)kJ/mol+(-c)kJ/mol=(a-b-c)kJ•mol-1,
故答案为:(a-b-c)kJ•mol-1.
