一定条件下,分别向容积固定的密闭容器中充入A和足量B,发生反应如下:2A(g)+B(s) 2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
2D(g)△H<0,测得相关数据如下,分析可知下列说法不正确的是
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
| 反应温度/℃ | 800 | 800 | 850 |
| c(A)起始/mol·L-1 | 1 | 2 | 1 |
| c(A)平衡/mol·L-1 | .0.5 | 1 | 0.85 |
| 放出的热量/kJ | a | b | c |
A.实验III的化学平衡常数K<1
B.实验放出的热量关系为b>2a
C.实验III在30min达到平衡时的速率v(A)为0.005mol• L-1·min-1
D.当容器内气体密度不随时间而变化时上述反应达到平衡
答案:B
题目分析:A、 2A(g)+B(s) 2D(g)
2D(g)
起始浓度(mol/L) 1 0
转化浓度(mol/L) 0.15 0.15
平衡浓度(mol/L) 0.85 0.15
所以该温度下反应的平衡常数K=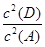 =
=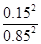 <1,因此A正确;
<1,因此A正确;
B、由于反应前后体积不变,所以实验I和实验Ⅱ的平衡是等效的,因此b=2a,B不正确;C、实验III在30min达到平衡时的速率v(A)=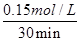 =0.005mol• L-1·min-1,C正确;D、密度是混合气的质量和容器容积的比值,在反应过程中质量是变化的,而容器容积是不变的,因此当容器内气体密度不随时间而变化时上述反应达到平衡,D正确,答案选B。
=0.005mol• L-1·min-1,C正确;D、密度是混合气的质量和容器容积的比值,在反应过程中质量是变化的,而容器容积是不变的,因此当容器内气体密度不随时间而变化时上述反应达到平衡,D正确,答案选B。
