开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池.
(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ•mol-1
③H2O(g)=H2O(l)△H3=-44.0kJ•mol-1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______.
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)⇌CO(g)+3H2(g)
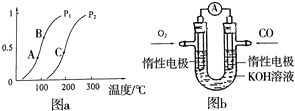
①一定条件下CH4的平衡转化率与温度、压强的关系如图a.则,Pl______P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为______.(填“<”、“>”“=”)
②100℃时,将1molCH4和2molH2O通入容积为100L的反应室,反应达平衡的标志是:______.
a.容器内气体密度恒定
b.单位时间内消耗0.1molCH4同时生成0.3molH2
c.容器的压强恒定
d.3v正(CH4)=v逆(H2)
如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K=______
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为______.用该原电池做电源,常温下,用惰性电极电解200mL饱和食盐水(足量),消耗的标准状况下的CO224mL,则溶液的pH=______.(不考虑溶液体积的变化)
(4)氢氧燃料电池的三大优点是:______、______、能连续工作.
(1)已知:①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ/mol
③H2O(g)═H2O(l)△H=-44.0kJ/mol
由盖斯定律,①-②+③×4得:
2CH3OH(l)+2O2(g)═2CO(g)+4H2O(l),故△H=-1275.6kJ∕mol-(-566.0kJ/mol)+(-44.0kJ/mol)×4=-885.6kJ∕mol,
所以其热化学反应方程式为:CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-442.8kJ∕mol,
故答案为:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=-442.8kJ•mol-1;
(2)①根据一定条件下CH4的平衡转化率与温度、压强的关系图知道,温度不变,则增大压强,平衡CH4(g)+H2O(g)⇌CO(g)+3H2(g)逆向移动,甲烷的转化率减小,所以Pl<P2,压强不变升高温度,甲烷的转化率会增大,平衡正向进行,所以反应是吸热反应,温度越高,K越大,A、B、C三点处对应的温度是逐渐升高的,所以平衡常数(KA、KB、KC)的大小顺序为KC>KB>KA,
故答案为:<;KC>KB>KA;
②a.容器内气体密度=
,质量是守恒的,V是不变的,所以密度始终不变,当密度不变时,不一定平衡,故错误;m V
b.单位时间内消耗0.1molCH4同时生成0.3molH2,只能说明正反应速率,不能证明正逆反应速率相等,不一定平衡,故错误;
c.反应是前后系数和变化的反应,当容器的压强恒定,则达到了平衡,故正确;
d.3v正(CH4)=v逆(H2),能体现v(正)=v(逆),故正确.
故选cd.
CH4(g)+H2O(g)⇌CO(g)+3H2(g)
初始浓度:0.01 0.0200
变化浓度:0.005 0.0050.0050.015
平衡浓度:0.0050.015 0.0050.015
所以平衡常数K=
=2.25×10-4(mol/L)2,0.0153×0.005 0.005×0.015
故答案为:cd;2.25×10-4(mol/L)2;
(3)在CO(g)、O2(g)、KOH(aq)设计成的燃料电池装置中,CO发生氧化反应,在负极失去电子,碱性条件下生成碳酸根与水,负极电极反应式为:CO-2e-+4OH-=CO32-+2H2O,用该原电池做电源,常温下,用惰性电极电解200mL饱和食盐水(足量),当消耗的标准状况下的CO224mL极0.01mol时,转移电子是0.02mol,根据电解氯化钠的反应方程式:2NaCl+2H2O
2NaOH+Cl2↑+H2↑,当转移电子是0.02mol时,生成氢氧化钠的物质的量是0.02mol,所以氢氧化钠浓度是通电 .
=0.1mol/L,即pH=13,故答案为:CO-2e-+4OH-=CO32-+2H2O;13.0.02mol 0.2L
(4)原电池具有能量利用率高的特点,氢氧燃料电池的产物是水,无污染,环保,故答案为:能量利用率高;无污染,环保.
