设反应①Fe(s)+CO2(g) FeO(s)+CO(g)△H=Q1的平衡常数为K1,
FeO(s)+CO(g)△H=Q1的平衡常数为K1,
反应②Fe(s)+H2O(g) FeO(s)+H2(g)△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g)△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
| 温度(T) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g)△H=Q3
CO(g)+H2O(g)△H=Q3
①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________。
A.缩小容器体积 B.降低温度 C.使用合适的催化剂
D.设法减少CO的量E.升高温度
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3=_____________;
(1)吸热
(2)①K3=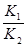 吸DE②Q3=Q1―Q2
吸DE②Q3=Q1―Q2
题目分析:
(1)对于反应①来说,升高温度其平衡常数增大,说明平衡正向移动,依据平衡移动原理:如果改变影响化学平衡的一个条件,那么平衡就向着能够减弱这种改变的方向移动,可知:正向是吸热的方向。
(2)反应①减去反应②就可以得到反应③:H2(g)+CO2(g) CO(g)+H2O(g)△H=Q3;因此反应应③的K3=
CO(g)+H2O(g)△H=Q3;因此反应应③的K3=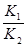 ;从表中的数据可知,随着温度的升高,K3的值是逐渐升高的,因此该反应是吸热反应;缩小容器体积,平衡不移动;降低温度,平衡逆向移动;使用合适的催化剂,平衡不移动;设法减少CO的量,减小了生成物的浓度,平衡右移;升高温度,平衡向着吸热的方向移动,因此选DE②Q3=Q1―Q2
;从表中的数据可知,随着温度的升高,K3的值是逐渐升高的,因此该反应是吸热反应;缩小容器体积,平衡不移动;降低温度,平衡逆向移动;使用合适的催化剂,平衡不移动;设法减少CO的量,减小了生成物的浓度,平衡右移;升高温度,平衡向着吸热的方向移动,因此选DE②Q3=Q1―Q2
